CRISPR-Cas9可以通過多種方法遞送���,包括質(zhì)粒����、重組病毒��、gRNA-Cas9 RNP復(fù)合物�,以及gRNA和Cas9 IVT mRNA的混合物,而這些方法都有各自的優(yōu)勢和局限性��。研究人員應(yīng)選擇適合自己實(shí)驗(yàn)應(yīng)用的遞送方法��,旨在通過最小化脫靶效應(yīng)和不良效果獲得最佳的編輯效率����,而IVT RNA正迅速成為其中一種效果良好的基因編輯工具��。
質(zhì)粒的大量制備一般成本較低��,并且可以通過技術(shù)相對簡單的化學(xué)轉(zhuǎn)染和電穿孔進(jìn)行遞送�����。然而�,由于這些遞送方式的自身特性�����,使得質(zhì)粒載體主要限于體外應(yīng)用�。此外,質(zhì)粒轉(zhuǎn)染的效率在不同細(xì)胞類型之間差異很大�����,且轉(zhuǎn)基因表達(dá)依賴于特定細(xì)胞類型的啟動(dòng)子活性�,而這在某些系統(tǒng)中可能會(huì)降低轉(zhuǎn)基因的表達(dá)效率。因此�,質(zhì)粒系統(tǒng)傾向配合使用高活性的啟動(dòng)子以確保Cas9的高水平表達(dá),但是這也會(huì)增加脫靶效應(yīng)和質(zhì)粒DNA隨機(jī)整合到宿主基因組中的風(fēng)險(xiǎn)�����。
重組病毒是遞送CRISPR-Cas9的另一種常用工具�����,特別適合難以轉(zhuǎn)染的細(xì)胞類型���,并且可以創(chuàng)建穩(wěn)定表達(dá)Cas9的細(xì)胞系以用于需要導(dǎo)入多個(gè)gRNA的實(shí)驗(yàn)�����。然而�����,該系統(tǒng)同樣與質(zhì)粒遞送系統(tǒng)一樣存在諸多相同的限制��,包括依賴特定細(xì)胞類型的啟動(dòng)子���,以及由于長期表達(dá)Cas9而導(dǎo)致的脫靶效應(yīng)風(fēng)險(xiǎn)增加。此外��,重組病毒也會(huì)帶來較高的插入突變風(fēng)險(xiǎn)�,特別是在逆轉(zhuǎn)錄病毒和慢病毒系統(tǒng)中的Cas9基因整合細(xì)胞基因組的時(shí)候���。
通過gRNA-Cas9 RNP復(fù)合物遞送可以繞過質(zhì)粒和重組病毒系統(tǒng)的許多限制,同時(shí)實(shí)現(xiàn)快速編輯�,因?yàn)椴恍枰M(jìn)行轉(zhuǎn)錄或翻譯。然而����,由于需要使用電穿孔方式實(shí)現(xiàn)高效的遞送,這種方法同樣主要限于體外應(yīng)用����。通過這種方法進(jìn)行的基因編輯發(fā)生得很快,但隨著Cas9在宿主細(xì)胞中被降解�����,編輯效果會(huì)迅速減弱�,因此常受到可用的Cas9蛋白的類型限制。
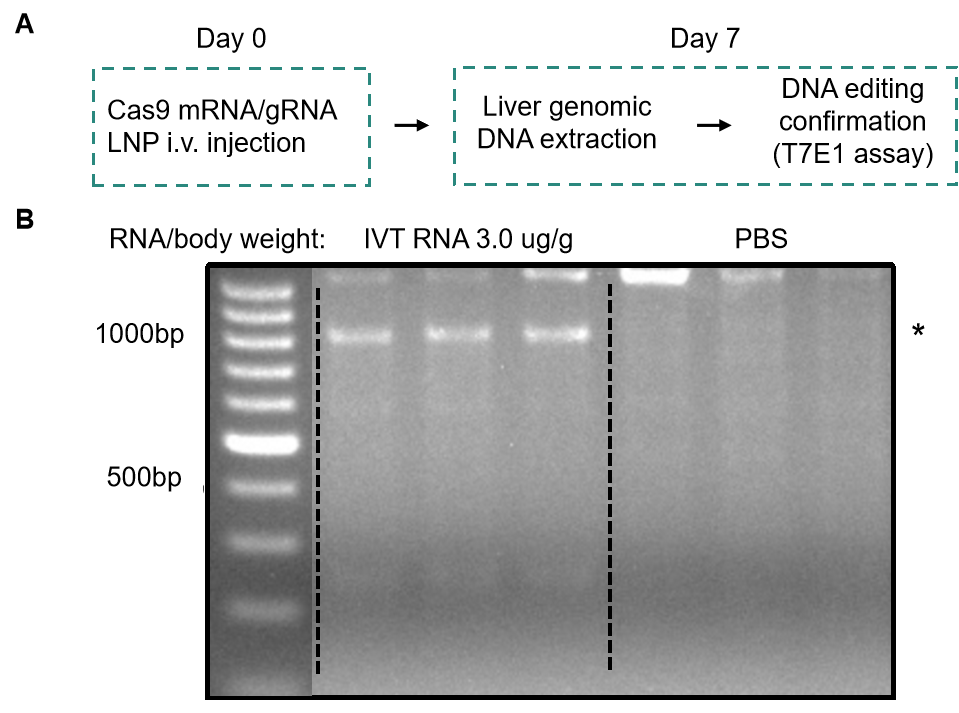
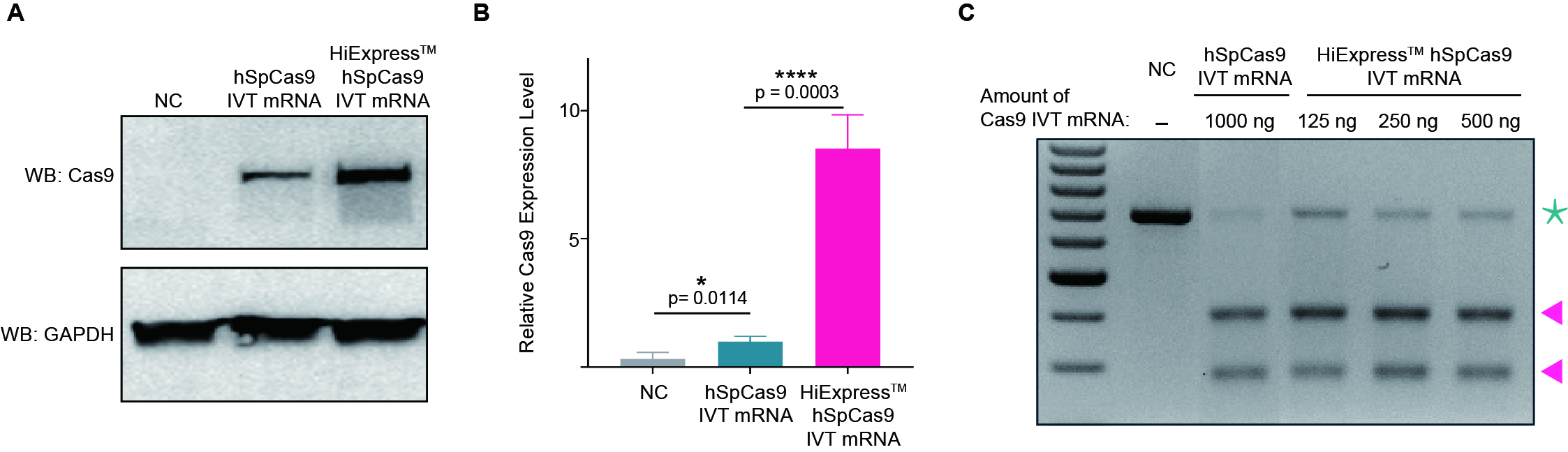
與上述方法相比��,使用gRNA和Cas9 IVT mRNA的混合物進(jìn)行遞送當(dāng)前已被認(rèn)為同樣是一種高效的基因編輯方法�����,具有最小化脫靶效應(yīng)的優(yōu)點(diǎn)��。該方法中,gRNA和Cas9 IVT mRNA一起被封裝在脂質(zhì)納米顆?���;蚧瘜W(xué)轉(zhuǎn)染試劑中�,使得該系統(tǒng)適用于體外和體內(nèi)應(yīng)用,并且無需擔(dān)心存在整合宿主基因組的風(fēng)險(xiǎn)�。此外,由于不需要進(jìn)行轉(zhuǎn)錄�����,轉(zhuǎn)基因的表達(dá)不依賴于特定的細(xì)胞類型啟動(dòng)子活性�����,翻譯的發(fā)生也相對更快���,從而實(shí)現(xiàn)快速且高效的基因編輯��。與gRNA-Cas9 RNP復(fù)合物相比����,mRNA形式的Cas9基因具有更長的表達(dá)時(shí)長��,可達(dá)成充分的基因編輯效果。然而����,mRNA最終也會(huì)被降解,編輯僅暫時(shí)發(fā)生過��,從而限制了脫靶效應(yīng)的影響�。
總而言之,通過質(zhì)粒��、重組病毒和gRNA-Cas9 RNP復(fù)合物遞送CRISPR-Cas9組分的方法均存在較多限制�����,對它們在許多場景中的應(yīng)用造成了阻礙�����。這些方法具有明顯的缺點(diǎn)����,包括相對有限的編輯效率、較高的脫靶效應(yīng)風(fēng)險(xiǎn)以及插入突變的潛在風(fēng)險(xiǎn)等�����。相對地,基于gRNA和Cas9 IVT mRNA混合物的遞送方式具有諸多優(yōu)點(diǎn)和較少的限制���,是一種高效的基因編輯方法����,應(yīng)更多地被考慮用于基因編輯實(shí)驗(yàn)��。